王伟课题组报道应激颗粒实现胞内氧化还原异质性的新功能:细胞抗氧化的“智能调控枢纽”
2025年12月19日,北京大学基因功能研究与操控全国重点实验室、生命科学联合中心王伟研究员在《Molecular Plant》期刊上在线发表了题为“Duet between stress granules and glutathionylation regulates cytosolic redox state to maintain proteostasis in Arabidopsis”的研究论文。该研究首次阐明蛋白谷胱甘肽化修饰与应激颗粒(Stress Granule,SG)的双向协同调控机制,不仅破解了细胞氧化平衡难题,更重新定义了SG的作为无膜细胞器整体的生物学新功能。

细胞内氧化应激是一柄双刃剑,适度氧化是能量代谢、信号传导的必需环节,但过度氧化则会导致蛋白损伤甚至降解,威胁细胞生存[1]。还原型谷胱甘肽(GSH)作为细胞核心抗氧化分子[2],其高达毫摩尔级含量如何得到精准的调控是长期以来领域内的未解之谜:如何在保障必要氧化反应的同时,避免蛋白氧化[3]?这一关键科学问题近日迎来突破性解答。
研究人员前期研究发现,在水杨酸(Salicylic Acid,SA)诱导的氧化应激条件下,细胞会大量形成由RNA与蛋白组成的SG,这类无膜细胞器可招募mRNA及翻译相关元件,从而调控应激状态下的细胞翻译水平[4]。在此基础上,研究人员进一步观察到,SG同时富集了大量与GSH合成及代谢相关的酶及蛋白,提示其可能参与细胞氧化还原调控。
为进一步深入研究SG的功能和GSH调控的细胞内氧化还原关系,研究人员开发了基于激活型荧光探针的点击化学反应实现了蛋白质谷胱甘肽化修饰的活体成像技术(Click-activated metabolic Labeling and imaging of glutathionylation,CamLog)。该技术无需转入外源基因,可实现天然生理条件下谷胱甘肽化修饰蛋白的动态可视化。借助CamLog技术,研究人员成功在拟南芥根部观察到SA诱导形成的谷胱甘肽化蛋白凝聚体。
接着研究人员通过SG标志蛋白共定位、SG富集蛋白的谷胱甘肽化修饰与质谱鉴定,证实了这些凝聚体是SG的核心组成部分。机制研究显示,SG的形成依赖蛋白液-液相分离(LLPS),而过度氧化会削弱蛋白的LLPS能力。SA诱导的蛋白谷胱甘肽化修饰,可赋予蛋白氧化还原缓冲能力,确保其在氧化环境中维持LLPS活性,进而促进SG组装。实验证实,利用TCEP抑制全局蛋白谷胱甘肽化修饰,可显著抑制SG的形成,明确了该修饰是驱动SG组装的关键分子基础。
随后研究人员揭示了SG的双重调控机制。作为无膜细胞器,一方面SG能在氧化态细胞质中构建还原性微环境,对翻译有关蛋白进行隔离保护,从而抑制氧化诱导的蛋白降解,例如抑制SG标记蛋白RBP47B的谷胱甘肽化修饰,不仅降低了SG的流动性,还抑制了植株对SA响应。另一方面,SG招募GSH生物合成的限速酶GSH1,通过抑制细胞质中的GSH合成,维持应激状态下的适度氧化水平,保障氧化信号通路的正常激活。
这一发现重新定义了SG作为无膜细胞器的整体性生物学功能,表明SG并不仅仅只是应激条件下的翻译调控场所,也是主动调控细胞抗氧化能力的核心枢纽。同时,SG与谷胱甘肽化修饰协同作用塑造的细胞质中氧化还原电势异质性,打破了人们对细胞抗氧化机制的传统认知,为重新理解细胞抗氧化机制提供了全新理论,也对易受氧化损伤的组织研究具有重要启示。近年来,谢周丽副教授的工作(Nature Plants,2023[4];Molecular Cell,2024[5];Molecular Plant,2025)系统解析了SG的功能机制,其研发的技术方法与提出的理论模型,为该领域研究提供了重要指导。
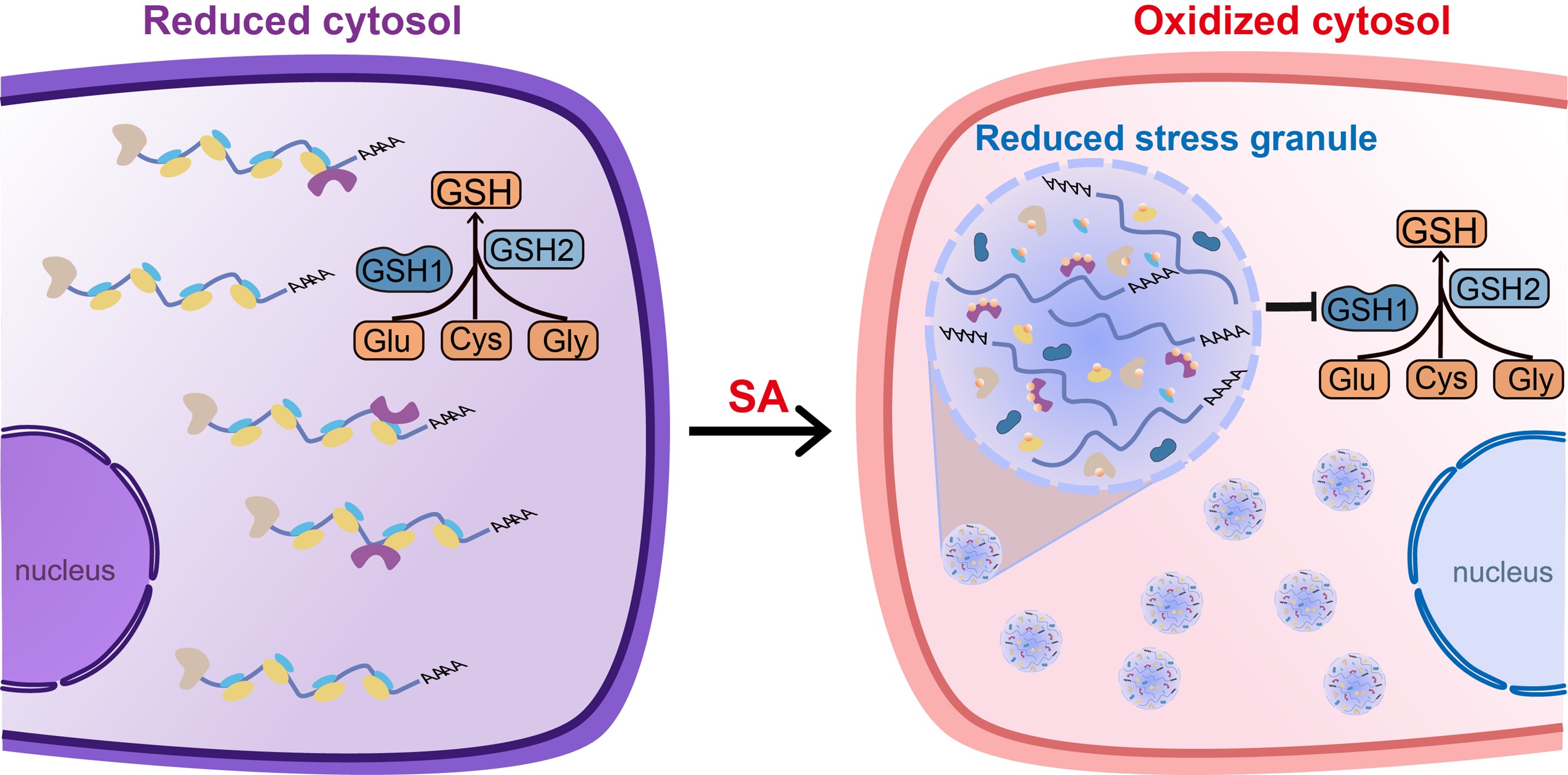
图. SG与谷胱甘肽化修饰协同作用,塑造出氧化还原电势的空间异质性分布
北京大学生命科学学院、基因功能研究与操控全国重点实验室、生命科学联合中心王伟研究员为论文通讯作者。北京大学博士后赵帅(已出站,现就职于首都师范大学)、博士后谢周丽(已出站,现就职于华中农业大学)和在读博士生陈効远为该论文的共同第一作者;首都师范大学周冕研究组参与了本研究。本研究得到了国家自然科学基金、基因功能研究与操控全国重点实验室、生命科学联合中心、首都师范大学、北京市自然科学基金、北京市科技新星计划和海外交流引进博士后等项目的资助。
原文链接:https://doi.org/10.1016/j.molp.2025.12.018
参考文献:
1. Waszczak, C., M. Carmody, and J. Kangasjärvi, Reactive Oxygen Species in Plant Signaling. Annu Rev Plant Biol, 2018.69: p. 209-236.
2. Noctor, G., et al., Glutathione in plants: an integrated overview. Plant Cell Environ, 2012.35(2): p. 454-84.
3. Noctor, G., J.-P. Reichheld, and C.H. Foyer, ROS-related redox regulation and signaling in plants. Seminars in Cell & Developmental Biology, 2017.80: p. 3-12.
4. Xie, Z., et al., Phenolic acid-induced phase separation and translation inhibition mediate plant interspecific competition. Nature Plants, 2023.9: p. 1481-1499.
5. Xie, Z., et al., Proteasome resides in and dismantles plant heat stress granules constitutively. Mol Cell, 2024.84(17): p. 3320-3335 e7.
- 钟声团队揭示被子植物配子互作的新机制2026.05.08
- 王伟课题组与合作者揭示大豆孢囊线虫劫持大豆生物钟的新机制2026.05.08
- 邓伍兰课题组首创 SMLDM 显微技术:单帧解析单分子定位与扩散,突破活细胞动态成像瓶颈2026.04.30
- 张蔚课题组与合作者揭示潮间带蜘蛛跨越陆海界限极端生存的基因组策略2026.04.28
- 陆剑研究组合作开发免疫印迹数学模型DynaVac,定量指导疫苗更新与接种策略2026.04.20
- 汪阳明团队开发REDDIT技术,实现增强子RNA与多类非编码RNA转录的高灵敏动态监测2026.04.20
- 陆剑课题组揭示果蝇上游开放读码框的演化规律与补偿机制2026.03.27
- 魏文胜课题组受邀综述:利用碱基与引导编辑器实现疾病相关变异的大规模解码2026.03.23
- 焦雨铃研究组构建禾本科花序发育数学模型,指导小麦高产基因挖掘2026.03.16
- 何爱彬团队与合作者开发新一代表观液体活检平台实现疾病组织器官精准溯源2026.03.05
- 陈雪梅教授课题组揭示新型RNA帽子修饰的跨物种分布与动态调控2026.03.05
- 肖俊宇团队与赵明辉、谭颖团队合作揭示补体系统C3转化酶组装及识别底物C3的分子机制2026.02.21
- 钟声课题组鉴定到拟南芥隔膜处“阻止多花粉管穿出”受体复合物的新组分2026.02.11
- 钟声研究员与瞿礼嘉院士合作揭示被子植物两次受精事件对受精补偿效率的关键作用2026.02.11
- 陈雪梅研究组揭示RdDM通路在作物免疫调控中的新功能,为大豆抗病改良提供了潜在的新思路、新靶点2026.02.10
- 秦跟基课题组揭示调控种子大小的新机制2026.02.10
- 罗述金课题组古DNA研究揭示:日本晚更新世并无虎,而为洞狮2026.01.27
- 张蔚课题组与合作者揭秘蜘蛛纺器起源2026.01.15
- 伊成器研究组报道AIM平台,突破“单点编辑”限制,实现RNA多位点、多功能精准操控2026.01.07
- 田望课题组发现植物抗逆“全能选手”,为提高植物“钙营养”和复合逆境抗性提供新概念2026.01.06
- 张蔚课题组与合作者揭示红珠凤蝶马兜铃酸抗性机制2026.01.05
- 刘君团队开发FOCAS平台实现m6A修饰位点的全转录组功能解析2026.01.05
- 肖俊宇研究组揭示FcRL5受体识别 IgG的分子机制2026.01.02
- 王伟课题组报道应激颗粒实现胞内氧化还原异质性的新功能:细胞抗氧化的“智能调控枢纽”2025.12.22
- 李晟课题组与合作者揭示保护地缓解人类对兽类行为干扰的关键作用2025.12.15
- 姚蒙研究组系统评估无脊椎动物宏条形码引物,助力eDNA生物多样性研究2025.12.12
- 朱丹萌课题组与合作者揭示PICKLE调控染色质状态与基因转录的分子机理2025.12.09
- 季雄团队提出FeaSion策略揭示RNA聚合酶磷酸化的特征调控与功能2025.12.01
- 罗述金课题组古DNA研究揭示:豹猫与人共栖3500年直至汉末,家猫经丝绸之路唐代方始传入2025.11.28
- 白洋研究员入选第三期 “新基石研究员项目”资助名单2025.11.26
- 实验室主任瞿礼嘉教授2025年新当选中国科学院院士2025.11.25
- 汪阳明团队与西湖大学卢培龙团队利用人工智能辅助蛋白质设计实现精准线粒体DNA碱基编辑2025.11.18
- 肖俊宇和高宁团队联合发表多聚抗体设计策略2025.11.07
- 赵进东课题组应邀撰写藻胆体的结构和能量传递机制长文综述2025.10.28
- 郑晓峰课题组揭示代谢酶ALDOA入核激活NF-κB信号通路驱动胰腺癌进展2025.10.23
- 陆剑课题组揭示果蝇饥饿耐受的遗传架构和性别差异2025.09.29
- 遇赫课题组揭示中国家猪的起源传播与人群互动过程2025.09.26
- 季雄团队揭示INO80/SWR复合物通过BRD2和染色质景观调控Pol II转录起始2025.09.22
- 刘启昆课题组与合作者在Current Opinion in Plant Biology发文总结植物再生领域表观遗传调控的研究进展2025.09.18
- 钟上威课题组受邀发表植物光信号传导Tansley长文综述2025.09.16
- 姚蒙课题组研发新型空气eDNA采集器高效检测动植物多样性2025.09.11
- 焦雨铃研究组克隆了小麦粒重新基因,服务高产育种2025.09.02
- 魏文胜团队与合作者联合开发新型通用型CAR-T 疗法治疗血液系统恶性肿瘤2025.08.22
- 魏文胜团队开发RNA环化新方法2025.08.12
- 汪阳明团队创新双组学技术MAPIT-seq:在单细胞水平同时绘制RNA结合蛋白作用图谱与基因表达图谱的新利器2025.08.11
- 周岳课题组揭示拟南芥PRC1介导的H2Aub loop的形成机制及功能2025.08.11
- 贺新强课题组与周岳课题组合作揭示PRC2调控维管组织模式建立机制2025.08.11
- 苏晓东课题组揭示清道夫受体CD163识别底物的分子机制2025.07.23
- 陈雪梅课题组系统阐释植物miRNA成熟与功能调控机制2025.07.23
- 苏晓东课题组与合作者揭示AAV与新型受体(AAVR2)结合的分子机制2025.07.15
- 合成植物基因组2025.07.09
- 伊成器课题组与合作者建立RNA"暗码",升级生命语言2025.07.04
- 魏文胜团队系统揭秘人类基因组中“沉默突变”的功能性“低语”2025.06.26
- 肖俊宇团队与张永辉团队合作揭示嗜乳脂蛋白激活γδ T细胞的“分子钳”机制2025.06.12
- 昌增益课题组揭示蛋白质内源性(顺式)去组装元件调控细菌细胞分裂环(Z环)的动态形成2025.06.09
- 陆剑课题组揭示uORF在动物进化与发育中发挥“翻译减震器”调控作用的新机制2025.06.09
- 张蔚课题组与合作者揭示兰花螳螂程序性体色转变的分子机制及生态学意义2025.05.30
- 2025年“全国科技活动周”和“全国科技工作者日”活动2025.05.29
- 李川昀团队与合作者开发细胞通讯分析工具STCase,揭示肿瘤微环境中空间特异性通讯事件2025.05.29
- 伊成器课题组系统阐释假尿嘧啶修饰的功能与治疗应用新范式2025.05.27
- 瞿礼嘉/钟声团队应邀撰写被子植物雌-雄相互作用保证双受精成功综述2025.05.26
- 陆剑课题组与合作者共同揭示uORFs通过精细调节CLOCK蛋白的翻译参与果蝇昼夜节律及睡眠行为的调控机制2025.05.16
- 伊成器团队发展痕量样品m6A修饰定量测序方法2025.05.08
- 白洋团队联合多位顶尖科学家系统解析根际微生物组调控水稻分蘖的功能与机制2025.04.24
- 瞿礼嘉/钟声课题组发现植物传粉过程中“未雨绸缪”的“两步授粉”备份新机制,为作物逆境下的育性优化提供新思路2025.04.15
- 曾虎课题组应邀撰写综述:空间组学技术的研究进展2025.04.06
- 张迪课题组受邀综述蛋白质L-乳酰化的研究进展2025.04.04
- 苏晓东课题组揭示短序列锚定元件AE在DNA与蛋白质结合中的重要作用2025.03.31
- 魏文胜团队实现人类肿瘤免疫调控网络的单碱基精度解析2025.03.21
- 白洋团队构建全球首个作物根际"细菌+病毒"基因组数据库2025.03.13
- 季雄团队揭示RNA聚合酶亚基RPB7偶联磷酸酶CTDP1稳定Pol II并介导转录再起始2025.03.05
- 何爱彬团队利用全景单细胞组蛋白修饰实现胚胎发育谱系追踪2025.03.04
- 赵进东课题组揭示蓝细菌藻胆体与光系统II结合的新分子机制2025.02.17
- 高歌课题组提出面向大规模异质性空间转录组学切片的表征与解析新方法2025.02.12
- 周岳课题组揭示拟南芥雄性生殖细胞发育过程中染色质三维结构的动态变化过程及其重要作用2025.02.12
- 魏文胜团队发布新一代线粒体碱基编辑器助力建立疾病动物模型2025.01.23
- 贺新强课题组揭示木质部管状分子发育的microRNA调控网络2025.01.19
- 周岳课题组在Genome Biology发文揭示了拟南芥中启动子空间调控模式和喷泉结构形成机制2025.01.02
- 高歌课题组提出人类转录调控元件建模与相关非编码变异功能解析方法2025.01.02
- 魏文胜团队利用碱基编辑器筛选绘制DNA损伤应答功能元件图谱2024.12.16
- 秦跟基课题组揭示弱光下种子萌发调控新机制2024.12.05
- 刘启昆课题组开发了全新的植物细胞谱系追踪工具2024.11.26
- 周岳课题组揭示植物首个三维基因组结构蛋白及其调控机制2024.11.22
- 周岳课题组揭示植物特有的PWWP结构域蛋白调控基因表达的分子机制2024.11.22
- 国家重点实验室陈雪梅教授获得2024年度“求是杰出科学家奖”2024.11.08
- 秦跟基课题组应邀撰写品牌综述“Tansley insight”总结TCP转录因子在细胞器、细胞和器官命运决定中的重要功能2024.10.28
- 郑晓峰课组揭示USP1-ATF4-CD98hc调控ENKTL淋巴瘤患者耐药的新机制2024.09.30
- 肖俊宇课题组揭示IgM–CD5L复合物的分子机制2024.09.30
- 陆剑课题组揭示密码子使用偏好性对翻译调控的影响2024.09.30
- 魏文胜团队实现蛋白质组中丝氨酸、苏氨酸和酪氨酸位点的功能解析2024.09.24
- 王继纵/邓兴旺课题组合作解析植物光敏色素phyB光信号转导的机制2024.09.24
- 刘君/杨雪瑞课题组合作揭示m6A-cenRNA调控癌细胞着丝粒稳态的机制2024.09.23
- 伊成器教授荣获2024年“科学探索奖”2024.08.29
- 王伟课题组报道蛋白酶体调控SG稳态抵御高温胁迫的新机制2024.08.22
- 肖俊宇团队阐明IgE 高亲和力受体FcεRI 复合物的组装机制2024.08.22
- 朱玉贤院士团队发布首个棉花基因组完整图谱,阐述棉族独特折叠胚胎形成的分子与演化机制2024.08.16
- 李晴课题组报道了滞后链核小体组装和冈崎片段成熟的协同机制2024.08.13
- 魏文胜团队报道非脱氨酶依赖的嘧啶碱基编辑器TBE2024.08.03
- 李晴研究组与合作者报道真核DNA复制体介导的亲本组蛋白表观遗传信息继承新机制2024.08.02
- 张迪课题组与合作者共同报道区分蛋白质乳酰化修饰同分异构体的新方法2024.07.22